Zawartość
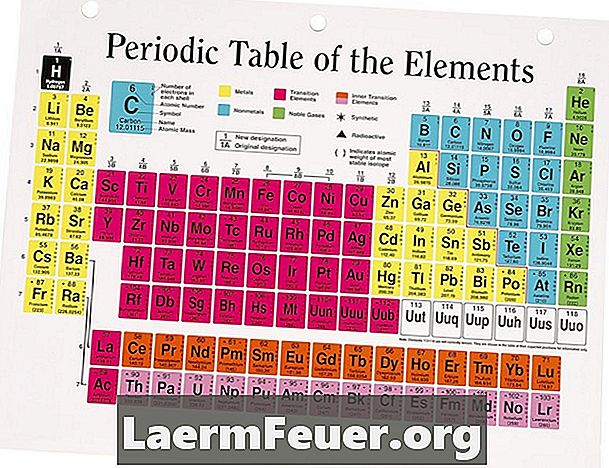
Elektrony walencyjne są elektronami najbardziej zewnętrznej warstwy, którą może wypełnić atom. Są znaczące, ponieważ zazwyczaj biorą udział w reakcjach chemicznych. Układ okresowy pierwiastków jest praktycznym odniesieniem do szybkiego określania liczby elektronów walencyjnych w atomie. Należy jednak zauważyć, że wiele elementów, z których większość to metale przejściowe, a nawet niektóre niemetale, może mieć kilka stanów walencyjnych, w zależności od konkretnego związku.
Instrukcje
-
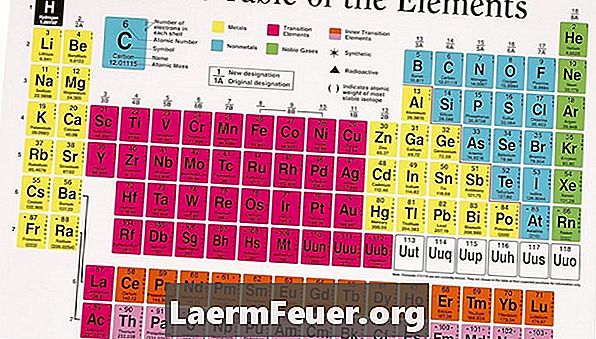
Znajdź element w układzie okresowym. Znajdują się w tabeli według liczby atomowej od lewej do prawej, od góry do dołu. Układ elementów w liniach odpowiada właściwościom dzielonym między nimi w danej kolumnie, znacznie zależnym od podobieństw w rozmieszczeniu tych elektronów.
-
Określ kolumnę, w której znajduje się element. Każda kolumna ma nazwę w pobliżu jej wierzchołka. System numeracji obecnie akceptowany przez IUPAC jest kolejno numerowany od 1 do 8. Wcześniej IUPAC nazywał kolumny 1A, 2A, 3A i tak dalej. Podczas gdy nowe tabele okresowe muszą zostać doposażone w nowy system, stare mogą korzystać z poprzedniej nomenklatury.
-
Policz liczbę kolumn od lewej do prawej, ignorując metale przejściowe i ostatnią kolumnę po prawej. Napisz to jako liczbę elektronów walencyjnych. Na przykład, używając poprzedniego systemu numerowania, po prostu wpisz cyfrę rzymską w kolumnie o nazwie liczby walencyjne elektronów, dla elementów w grupach IA, IIA, IIIA, IVA, VA, VIA i VIIA.
-
Napisz zero dla liczby elektronów walencyjnych dla elementów grupy 18 (dawniej zwanej grupą VIIIA). Elementy te stanowią najbardziej zewnętrzną wypełnioną warstwę elektronową i na ogół nie biorą udziału w reakcjach chemicznych.
-
Napisz słowo „zmienia się” dla elementów znajdujących się w bloku metalu przejściowego układu okresowego, ponieważ rozmieszczenie elektronów w tych elementach pozwala uczestnikom warstwy najbardziej wewnętrznej uczestniczyć w reakcjach chemicznych. To sprawia, że wydają się mieć wartościowość, która zmienia się w różnych reakcjach. Żelazo, na przykład, czasami reaguje za pomocą dwóch elektronów, a kolejne trzy, co daje pozorną wartość dwóch lub trzech.
Czego potrzebujesz
- Układ okresowy pierwiastków